Un videojuego permite diseñar una proteína más potente que la natural
Un laboratorio verifica los resultados de los prototipos elaborados por los usuarios de 'Foldit'
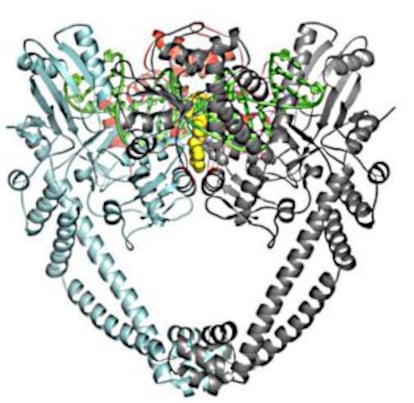
Los usuarios de un videojuego han conseguido ir un paso más allá en su ayuda a los investigadores. El programa Foldit empezó siendo una llamada para que los voluntarios dejaran que los sistemas informáticos que se dedican a estudiar el plegamiento de proteínas (la estructura tridimensional en que se pliega la cadena de aminoácidos) les prestaran la capacidad de sus ordenadores; de ahí pasó a ser interactivo, con los jugadores diseñando estas estructuras. Y, ahora, han ido un paso más allá, ensamblando las partes del puzle hasta conseguir moléculas artificiales hasta 18 veces más eficaces que las naturales. El resultado ha sido verificado en un laboratorio, y lo ha publicado Nature Biotechnology.
Una enzima –que es el caso sobre el que han trabajado- es una proteína que actúa como una especie de micromáquina molecular. Al igual que pasa con el ADN, las proteínas con macromoléculas: una secuencia de aminoácidos (lisina, arginina, tripsina, alanina…. y así hasta 23 eslabones). Pero solo con ponerlos en fila no se conseguiría nada. Lo que importa es cómo se pliega (como si se toma una cadena y se arroja al suelo). Pero este proceso no se puede realizar al azar. Cada uno de los eslabones tiene cargas electrónicas y otras características que hacen que unas estructuras tridimensionales sean más probables que otras, y, más importante aún, que determinan que la proteína cumpla su función o no.
Como una proteína puede tener 500 o más aminoácidos, predecir cuál será el plegamiento real es muy complejo. Esas son las reglas del juego Foldit, que crearon en 2008 Zoran Popovic y David Baker, de la Universidad de Washington en Seattle. Como en todos los programas, este se ha ido complicando, en su último reto ha ido más allá: no se trata de adivinar cuál es la forma de una molécula a partir de su secuencia obtenida de la naturaleza, sino que, dando los componentes posibles, se ha permitido construir una, cuya eficacia se ha probado en laboratorio.
En uno de los puzles, se preguntó a los participantes (hay unos 240.000 inscritos, con más de 2.000 activos por semana) que rediseñaran un bucle de cuatro aminoácidos de una enzima (un catalizador biológico) para que aumentara la superficie de contacto con uno de los reactivos. Luego, se les pidió que presentaran mejoras que estabilizaran esa estructura. El resultado fueron más de 70.000 propuestas para la primera parte, y 110.000 para la segunda. Los investigadores que estaban detrás del proyecto luego eligieron las respuestas que les parecieron mejores, y consiguieron enzimas 18 veces más eficaces que las naturales.
“He trabajado dos años para mejorar esas enzimas, pero no lo conseguí”, ha admitido Justin Siegel, un investigador de posdoctrado del grupo de Baker. “Los jugadores de Foldit, en cambio, consiguieron un gran salto en su estructura especial, y todavía no sé cómo lo han logrado”, admitió.
En este momento el hallazgo no tiene demasiadas aplicaciones prácticas. Pero eso tiene fácil arreglo. Baker ha dicho que ya ha planteado a los jugadores un nuevo reto: fabricar inhibidores más potentes para el virus de la gripe de 1918. "Y eso puede traducirse en medicamentos".