La terapia génica sale del túnel
Los últimos resultados impulsan el renacer de la técnica con virus más seguros En 2003 se pararon ensayos por casos de pacientes que desarrollaron leucemia
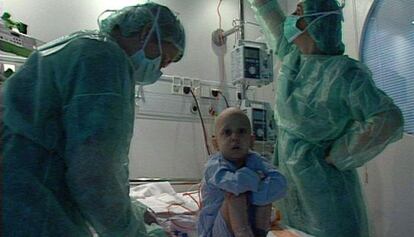
La primera alarma relacionada con la terapia génica saltó en Estados Unidos con la muerte de un paciente en 1999. Pero la caída en desgracia de la técnica llegó unos pocos años más tarde, con los casos de leucemia que desarrollaron dos menores tratados en Francia. Como consecuencia de ello, en 2003 se suspendieron casi una treintena de ensayos clínicos en Estados Unidos. Las esperanzas que despertó este procedimiento recibieron un rotundo revés mientras los investigadores la sometieron a una profunda revisión.
Casi una década después, la terapia génica comienza a salir del túnel. “Se está produciendo un avance espectacular en los últimos meses”, explica Juan Bueren, jefe de la división de hematopoyesis y terapia génica del Centro de Investigaciones Energéticas, Medioambientales y Tecnológicas (Ciemat) / CIBER de Enfermedades Raras. Sin hacer demasiado ruido y con la cautela que exige la experiencia reciente, media decena de ensayos en humanos están arrojando resultados ilusionantes en enfermedades que actualmente no tienen cura, como distintas inmunodeficiencias, hemofilia, beta-talasemia (una rara patología de la sangre) e incluso un tipo de ceguera hereditaria (amaurosis congénita de Leber).
La terapia génica de las enfermedades congénitas consiste en curar a los pacientes reparando el gen mutado que les provoca la patología que padecen. Para ello se les añade la copia del gen sano que les falta. O mejor, se les infecta, porque el fragmento de ADN que necesitan se inserta en la doble hélice a través de un virus modificado que transporta el gen encapsulado hasta su destino.
Una de las claves para que la terapia funcione consiste en encontrar el vehículo adecuado (vectores, en jerga científica) para trasladar e insertar el gen en el ADN del paciente. Y los virus empleados en los primeros ensayos eran poco precisos y poco seguros. Además de alojar la información genética que tiene que curar al enfermo, los vectores virales transportan una secuencia de activación destinada a que el gen se exprese y produzca la proteína de la que carece el paciente. En el caso de los afectados por hemofilia tipo A, por ejemplo, el gen F8 no produce el factor de coagulación VIII, una proteína que interviene en el proceso de coagulación de la sangre. El virus contendría una copia buena del F8 y algo así como una llave de contacto que enciende el motor del gen y lo pone en funcionamiento para que produzca el factor VIII.
"Se ha producido un avance espectacular”, explica el especialista Juan Bueren
Los investigadores se dieron cuenta de que, en los primeros virus empleados —del tipo retrovirus— , este interruptor no solo activaba el gen terapéutico transferido, sino que era tan potente que también podía arrancar la maquinaria de algunos de los genes adyacentes. De forma que si, en la larga cadena del ADN celular, el virus insertaba el gen en una zona cercana a un oncogen silenciado, era capaz de despertarlo y poner en marcha los mecanismos de desarrollo tumoral.
Esto es lo que sucedió en algunos ensayos. Había pacientes que se curaban. Pero otros desarrollaban leucemia, como sucedió con dos de los 13 menores con inmunodeficiencia grave combinada (conocidos como niños burbuja, por su necesidad de vivir en un entorno estéril debido a su desprotección frente a las infecciones) tratados en un trabajo francés que se suspendió en 2002.
Los nuevos vectores han solventado buena parte de los peligrosos inconvenientes que presentaban los primeros virus empleados. “Hace cinco años que tenemos vectores nuevos que están solventando los problemas de seguridad que había antes, aunque la explosión de la terapia se está produciendo ahora”, afirma Fátima Bosch, directora del Centro de Biotecnología animal y Terapia Génica de la Universidad Autónoma de Barcelona.
La técnica consiste en curar al implantar una copia sana del gen alterado
Por una parte, estos nuevos vectores tienen una menor tendencia a integrarse en zonas del ADN que potencialmente causan cáncer que los retrovirus. De hecho, hay estudios en ratones que han observado que los virus de última generación no aumentan ni la incidencia de tumores ni su aparición de forma temprana. Por otro lado, las nuevas secuencias reguladoras empleadas (los motores de arranque) son más débiles, “por lo que ya no existe tanto riesgo de activar genes peligrosos”, explica Bueren.
Estos nuevos vectores virales (los derivados de los adenovirus, como el del resfriado común, los lentivirus, como el VIH) son los que se han empleado en algunos de los ensayos que devuelven hoy la fe en la terapia génica a un número creciente de investigadores.
Entre los trabajos más recientes se encuentra el anunciado en diciembre del año pasado por el University College de Londres y el St. Jude Children’s Research Hospital estadounidense. Se trata de un trabajo con personas afectadas por la hemofilia B —el gen alterado en este caso es el F9 que da lugar al factor de coagulación IX—. En principio, es un caso ideal al que aplicar la terapia génica, ya que se trata de una enfermedad monogénica, por lo que bastaría con introducir y poner en funcionamiento el gen F9 sano para curar a estas personas.
Esto es lo que hicieron los investigadores que diseñaron el ensayo y que emplearon un virus adenoasociado para introducir el gen sano. Gracias a ello, los pacientes consiguieron aumentar la producción de factor de coagulación un 12%, suficiente para que no necesitaran las dos inyecciones semanales en que consiste el tratamiento de la enfermedad. “Lo más interesante del trabajo es que aún están en proceso de escalado [midiendo la dosis adecuada] y que a pesar de que se administraron dosis bajas, los resultados fueron satisfactorios”, asegura Bueren.
Otro de los ensayos “importantes” en terapia génica, comenta este investigador del Ciemat, está relacionado con el tratamiento de un raro caso de ceguera hereditaria que consiguió mejorar la visión en tres pacientes. Los resultados son aún más recientes —se presentaron el pasado mes de febrero— e incluso más sorprendentes.
La enfermedad que se abordó es la amaurosis congénita de Leber, que afecta a uno de cada 35.000 nacidos y que deja a quienes la padecen sin visión, como muy tarde, a los 40 años. Como en la hemofilia, el responsable de la patología es la mutación en un gen, el RPE65, que impide que el paciente produzca una proteína clave en el proceso de la visión. Sin ella, las células fotosensibles son incapaces de captar la luz y enviar las señales nerviosas que el cerebro interpreta.
El ensayo, diseñado por investigadores del Hospital Infantil de Filadelfia y la Universidad de Pensilvania, consistió en inyectar directamente en la retina de 12 personas la copia sana de información genética encapsulada en un adenovirus. Se inoculó en el ojo de peor visión y tres pacientes volvieron a ver con poca luz. En una segunda fase, los investigadores lo repitieron en el otro ojo. “Los pacientes ahora son capaces de ir de compras al supermercado y reconocer los rostros de la gente, algo que no podían hacer antes”, señaló Jean Benett, uno de los autores de la investigación.
La beta talasemia es otra enfermedad que se podría beneficiar de la terapia génica. De momento, investigadores del hospital de París y de Harvard consiguieron a finales de 2010 que un paciente con esta rara enfermedad de la sangre (los afectados no pueden producir glóbulos rojos sanos) no tenga que recurrir a transfusiones periódicas para sobrevivir. Varios años antes, cuatro equipos de científicos (franceses, ingleses, italianos y alemanes) lograron los primeros éxitos claros de este tipo de terapia al curar a pacientes con diferentes inmunodeficiencias graves.
Cuatro años antes, un equipo de investigadores alemanes logró el primer éxito claro de este tipo de terapia al curar a dos hermanos de una grave inmunodeficiencia (granulomatosis crónica ligada al cromosoma X).
Estos resultados van en la buena dirección y sirven para apuntalar la idea de que la terapia génica no solo cura, sino que se pueden controlar sus riesgos. Para que llegue ese momento, y este procedimiento deje de ser un tratamiento experimental, aún quedan por resolver distintos problemas. Uno de los que más preocupa a los investigadores consiste en asegurar que la información genética se inserta en el lugar deseado y evitar de esta forma que el virus descargue el gen en zonas sensibles. No solo por la posible presencia cercana de oncogenes. Solo el 3% del ADN contiene regiones codificantes (genes que expresan proteínas). Es una tasa baja, pero existe el riesgo de que el gen se inserte en medio de otro, con consecuencias desconocidas. “Existen grupos de investigación trabajando en vectores que se integren solo en zonas no codificantes”, indica Bueren.
Otra de las soluciones dirigidas a aumentar los márgenes de seguridad consiste en sustituir el gen defectuoso por uno nuevo, en lugar de insertar una copia sana en un lugar indeterminado de la doble hélice (con los riesgos que comporta). Es una técnica más segura, pero exige una gran precisión. Para ello se están desarrollando herramientas de ingeniería molecular como las llamadas tijeras de dedos de zinc, unas proteínas capaces de elegir el lugar del ADN del receptor donde cortar e insertar los genes reparados.
Sea cual sea el sistema de inserción guiada que resulte más eficaz, el objetivo será siempre el mismo. Conseguir la mayor fiabilidad de una técnica destinada a curar la enfermedad de raíz: atacando el gen defectuoso.
Virus del catarro programados contra el cáncer
Equipos de investigación españoles han diseñado cuatro ensayos clínicos relacionados con la terapia génica. Uno de los más espectaculares es el que dirige Manuel Ramírez, del hospital Niño Jesús de Madrid, el único que, de momento, ha sido aprobado por la Agencia Española del Medicamento.
“No es terapia génica al uso”, advierte Ramírez. El empleo de virus modificados (adenovirus del catarro diseñados por Ramón Alemany del Instituto Catalán de Oncología) no está destinado en este caso a insertar genes sanos que sustituyan la función de otros defectuosos. Su objetivo es atacar un tumor del sistema nervioso (neuroblastoma). “Estos virus son capaces de dividirse en las células tumorales, replicarse en progresión geométrica y literalmente reventarlas”, explica Ramírez, de forma que se diseminan y vuelve a comenzar el proceso. Además, tienen la propiedad de respetar a los tejidos sanos y se eliminan prácticamente sin toxicidad. En ensayos previos, se ha analizado la seguridad de la terapia, destinada a niños, y ha observado resultados esperanzadores. El nuevo ensayo está dirigido a estudiar la eficacia terapéutica.
El equipo de Juan Bueren del Ciemat / Ciberer tiene pendiente la aprobación de un ensayo dirigido a tratar pacientes con anemia de Fanconi, una enfermedad de la sangre. En este caso, la técnica sí se ajusta al procedimiento clásico de corregir un gen defectuoso. El proceso consiste en extraer las células del paciente alteradas (las hematopoyéticas, encargadas de producir glóbulos rojos, blancos y plaquetas) y corregirlas en el laboratorio mediante el contagio de un lentivirus (un vector de última generación), que repara el gen alterado. Una vez corregido el defecto genético, se reinfunden las células para que produzcan los distintos linajes celulares sanguíneos.
Otro ensayo, que ya cuenta con la colaboración de los Laboratorios Esteve, es el diseñado por Fátima Bosch, del centro de Biotecnología Animal y Terapia Génica de la Universidad Autónoma de Barcelona, para tratar la mucopolisacaridosis 3A, una enfermedad metabólica rara. El cuarto trabajo en curso lo desarrolla la Clínica Universitaria de Navarra y tiene que ver con otra patología muy poco frecuente que afecta al metabolismo, la profiria aguda intermitente.