El CNIO consigue reprogramar células madre embrionarias dentro del cuerpo
Su capacidad de diferenciación supera la conseguida en el laboratorio El trabajo sugiere la posibilidad futura de autoregeneración de tejidos lesionados
Desde que en 2009 se consiguió reprogramar simples células adultas de la piel para transformarlas en células madre iPS o pluripotentes, tan versátiles como las células madre embrionarias, este procedimiento siempre se había realizado en el laboratorio.
Un equipo del Centro Nacional de Investigaciones Oncológicas (CNIO) ha demostrado, por vez primera, que el proceso de retrasar el reloj de las células adultas (reprogramarlas) para convertirlas en iPS se puede provocar también en el organismo de un ser vivo adulto. Pero, además, estas células madre, que se han desarrollado en ratones, tienen mayor capacidad de diferenciación (de convertirse en distintos tejidos) que las obtenidas en laboratorio. Esta nueva técnica no tiene impacto terapéutico directo. Pero permite pensar en un futuro, aún lejano, en el que sean los propios órganos lesionados los que puedan producir células madre para regenerarse.
“Es un trabajo excepcional”, reflexiona Juan Carlos Izpisúa, director del Centro de Medicina Regenerativa de Barcelona. “Abre una nueva etapa para la medicina, la búsqueda de estrategias que nos permitan regenerar órganos y tejidos de una forma similar a los procesos naturales”.
El trabajo del grupo de Manuel Serrano, director del programa de Oncología Molecular del CNIO, lo publica Nature y parte de la técnica que le permitió al investigador japonés Shinya Yamanaka obtener células madre iPS en 2007 y el Nobel en 2012.
Yamanaka reprogramó las células adultas introduciendo en ellas cuatro genes característicos de la etapa embrionaria, de forma que, al activarse, devuelven a la célula a un estadio prácticamente igual al de una célula embrionaria, convirtiéndola en la famosa iPS. Serrano ha usado la misma combinación de genes, el llamado coctel Yamanaka, pero le ha dado varias vueltas de tuerca, con unos resultados sorprendentes e inesperados.
El equipo del investigador español diseñó un ratón al que introdujo un gen artificial que, en respuesta a la administración de un antibiótico —tetraciclina— se activa y produce el mismo efecto que el coctel de las cuatro proteínas de Yamanaka.
La intención original de Serrano no era generar células madre iPS en el interior de los roedores, sino algo “mucho más prosaico”, como traslada a este diario. Buscaba una forma sencilla de obtener células madre embrionarias. Y la forma de conseguirlas era extraer las células de los ratones con el genoma modificado, bañarlas en una placa de laboratorio con el antibiótico y generar fácilmente cultivos de células iPS.
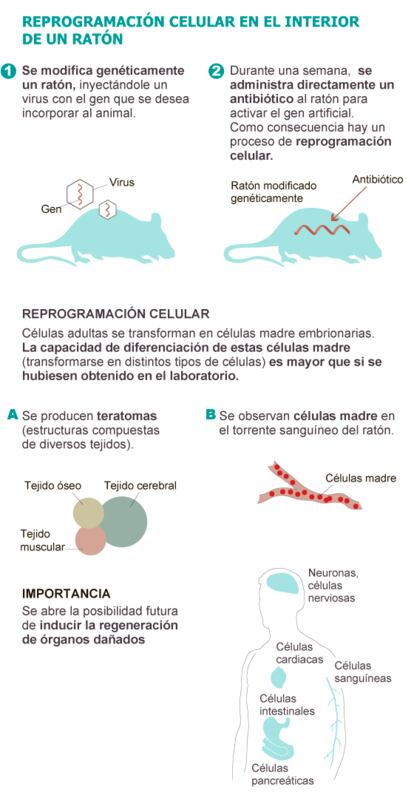
Pero en un momento dado, le surgió la duda. ¿Que sucedería si se administraba el antibiótico directamente al ratón modificado genéticamente y no a los cultivos de sus células? “Sinceramente, no confiábamos en que las células se fueran a reprogramar dentro del ratón”, traslada el investigador. "No creíamos que funcionara”, insiste. Pero funcionó.
Los ratones modificados de Serrano bebieron el antibiótico diluido en agua durante una semana. Al poner en marcha el mecanismo descrito por Yamanaka y adaptado por el CNIO, los investigadores observaron que células adultas de los ratones perdían sus características y adquirían rasgos de células embrionarias “que no existen en los organismos adultos”, destaca Serrano.
Tras retroceder, desprogramarse y convertirse en células madre, las células se replicaban de forma descontrolada y desordenada en el interior del cuerpo de los roedores dando lugar a una especie de masa compuesta de diferentes tejidos (cerebral, muscular, óseo, intestinal...) de tejidos. Una especie de embrión desorganizado denominado teratoma.
La importancia de estas estructuras pseudoembrionarias que aparecían por decenas en el tórax y en el abdomen no está en su utilidad clínica. Ninguna terapia puede pasar por provocar teratomas. Lo relevante es que de esta forma quedaba patente la elevada capacidad de diferenciación de las células madre generadas en el interior de los ratones. Estas estructuras no solo contenían células derivadas del desarrollo del embrión (de las tres capas que lo conforman), sino incluso de tejidos externos al embrión, como es el caso de saco vitelino.
Además, los investigadores del CNIO detectaron células madre en el torrente sanguíneo de los ratones tratados
En ambos casos —tanto en los teratomas como en la sangre— las células madre obtenidas presentaban unos estadios embrionarios aún más tempranos que las células producidas mediante la técnica de Yamanaka. Es decir, habían retrocedido a un nivel más primitivo, por lo que presentaban una mayor facultad de diferenciación en diferentes tipos celulares. Presentaban características de embriones humanos de tan solo 72 horas de gestación y 16 células, que en la jerga se denominan rasgos totipotentes.
Estas características de indiferenciación tan elevadas “nunca se habían generado en el laboratorio", según los autores. “Estos datos nos indican que nuestras células madre son mucho más versátiles que las células iPS de Yamanaka”, destaca Serrano. La contrapartida de esta facultad es que las células son más difíciles de controlar cuando llega el momento de convertirlas en tejidos concretos.
El objetivo de la medicina regenerativa consiste en curar órganos dañados a través de células sanas. La materia prima de este enfoque terapéutico son las células madre por su capacidad de convertirse en cualquiera de los más de 100 tipos celulares. Los especialistas aspiran a poder manipular estas células desprogramadas para convertirlas en células sanas de hígado, corazón o páncreas con las que tratar insuficiencias hepáticas, infartos o diabetes. O incluso desarrollar en el laboratorio órganos completos de repuesto para sustituir a los enfermos.
Las células iPS cumplen estas condiciones de versatilidad. Y, además, no plantean los problemas éticos que si presentan las células madre embrionarias humanas. Por ello, los investigadores del CNIO plantean que la nueva fuente de células madre que han descrito puede constituir una fuente alternativa a las que se obtienen en el laboratorio para la investigación en medicina regenerativa. “Nuestras células madre sobreviven también en cultivos fuera de los ratones”, apunta María Abad, primera autora del artículo.
Pero existe otra futura aplicación terapéutica más atractiva, aunque cuya aplicación se muestra mucho más remota. Se trataría de aprovechar la capacidad de crear células madre dentro del cuerpo para inducir la regeneración endógena en un área dañada.
En los procesos naturales de regeneración, las células sanas dirigen a las células reparadoras. En el trabajo de los investigadores españoles, como explica Serrano, la diferenciación inducida en las células adultas era tan alta que las células madre eran insensibles a las señales del entorno y desarrollaban teratomas.
Uno de los próximos objetivos de los investigadores del CNIO consiste en determinar si existe un grado de diferenciación que permita a las células madre iPS generadas interactuar con su entorno y reparar por sí mismas, desde dentro, el tejido lesionado. "Vamos a provocar daños en ratones, un infarto por ejemplo, y administrar menos medicación, de forma que exista un menor grado de reprogramación celular", comenta el investigador. “Queremos observar si esas células menos diferenciadas pueden dar lugar a cardiomiocitos que mejoren la función cardiaca”.
Este cambio de concepto, el de inducir la regeneración terapéutica en lugar de crear tejidos de repuesto en el laboratorio, evitaría riesgos derivados de las intervenciones quirúrgicas a las que se deberían someter los pacientes para recibir los órganos y tejidos reparadores. O accidentes en la manipulación de los cultivos, entre otros.
El grupo de Serrano no es el primero en plantear este enfoque. Un trabajo del Centro de Medicina Regenerativa de Barcelona y el Instituto Salk anunció hace casi dos meses una nueva fórmula para generar iPS en el laboratorio. En lugar de la receta Yamanaka (que consiste en despertar cuatro genes activos en la etapa embrionaria, dos de los cuales inducen a la formación de tumores), este grupo desarrolló un cóctel alternativo que pasaba por alterar otros siete genes que ya están activos en las células adultas. Ello abría la posibilidad reajustar la expresión de estos genes dentro del cuerpo para que generaran células madre reparadoras en los propios tejidos. La misma idea de la regeneración endógena órgano planteada por Serrano.
Todos estos planteamientos de la medicina regenerativa suenan aún a ciencia ficción. Y lo son. Aunque cada vez menos. Japón aprobó en junio el primer intento de llevarlos a la práctica. Autorizó un ensayo para crear retinas con células iPS para implantarlas en ciegos con degeneración macular.